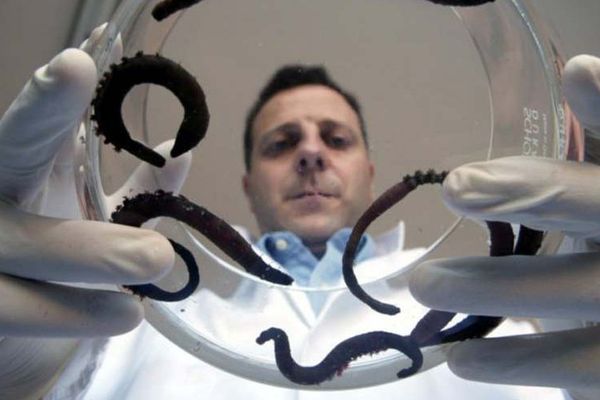
L'essai clinique, qui prévoyait d'administrer à des patients atteints du Covid-19 une solution issue du sang d'un ver marin, a été stoppé jeudi. L'une des autorisations délivrées vient d'être retirée dans l'attente d'une nouvelle évaluation.
L'essai clinique qui prévoyait d'administrer à des patients atteints du Covid-19 une solution issue du sang d'un ver marin a été stoppé jeudi, son autorisation ayant été retirée dans l'attente d'une nouvelle évaluation, a indiqué l'Assistance publique-Hôpitaux de Paris (AP-HP).
L'Agence du médicament (ANSM) a décidé de "suspendre en urgence" le feu vert qu'elle avait donné pour cette étude, après avoir pris connaissance de résultats négatifs
d'une étude précédente sur des porcs de cette solution aux pouvoirs d'oxygénation très importants, fabriquée par la société morlaisienne Hemarina.
En conséquence, "l'AP-HP a décidé de ne plus être promoteur" de cet essai clinique, explique le groupement hospitalier dans un bref communiqué, qui précise que "l'essai n'avait pas débuté et aucun patient n'a donc reçu ce produit expérimental."
Échec d'une précédente étude sur des porcs
"Il vient d'être porté à la connaissance de l'ANSM la réalisation en 2011 d'une étude non clinique chez le porc", qui s'est traduite par "une létalité de 100%" chez les animaux ayant reçu cette substance, observe le gendarme des médicaments dans sa décision, datée du 8 avril et transmise par l'AP-HP. Or les "résultats de cette étude n'ont pas été versés à l'ANSM dans le cadre de la demande d'autorisation de l'essai clinique", souligne l'agence, ajoutant qu'une "réévaluation (...) est nécessaire pour apprécier les risques encourus au regard du bénéfice escompté chez les patients".
Double feu vert accordé
L'AP-HP avait annoncé samedi le lancement de cet essai, qui avait reçu l'autorisation de l'ANSM le 27 mars et le feu vert d'un comité de protection des personnes le 3 avril. Hemo2life, le produit mis au point par l'entreprise morlaisienne Hemarina, utilise les étonnantes propriétés de l'hémoglobine d'arénicole (ver marin) en matière de transport d'oxygène vers les organes et les tissus.
Une première phase d'essais prévue sur 10 patients
Dix patients en état très grave, hospitalisés dans les services de réanimation de l'Hôpital européen Georges-Pompidou et de la Pitié-Salpêtrière, devaient se voir administrer ce produit pour évaluer s'il était bien toléré et s'il permettait d'améliorer l'oxygénation de leurs organes.
Les doses d'Hemo2life devaient être injectées par intraveineuse à des patients qui sont en insuffisance respiratoire, mais qui ne peuvent être ni intubés, ni placés sous ECMO (une machine qui permet d’oxygéner le sang artificiellement), car ce sont des dispositifs très lourds qu’ils ne supporteraient pas, en raison de leur âge ou de leur état de santé.
En outre, ces patients devaient aussi répondre à des critères précis : ne pas avoir de maladies du sang par exemple, et obtenir leur consentement (ou celui de la famille, si le patient est dans le coma.)
Hemarina déplore une décision "expéditive"...
Dans un communiqué publié en milieu d'après-midi, Hémarina déplore la décision "expéditive" de la direction de l'AP-HP de ne pas poursuivre cet essai, "alors que les informations demandées par l'ANSM ont été apportées". "Les éléments complémentaires demandées par l'ANSM dans sa décisions du 8 avril ont été fournis dès le 8 avril par Hemarina, à savoir les détails d'une étude préclinique de 2011 sur des modèles animaux. Cette étude préclinique portait sur un produit non pharmaceutique totalement différent du produit actuel (...)."
... et espère une nouvelle autorisation
Contactée, l'ANSM nous a expliqué que l'agence demandait des études complémentaires susceptibles d'aboutir à une nouvelle autorisation. Encore faudrait-il trouver un nouvel établissement hospitalier d'accord pour reprendre l'essai, l'AP-HP ayant, pour sa part, décidé de ne plus être promoteur de l'étude.
"Nous sommes confiants sur une autorisation rapide à venir de la part de l'ANSM, en collaboration avec un autre ou d'autres promoteurs cliniques à venir", commente Franck Zal, fondateur d'Hemarina.