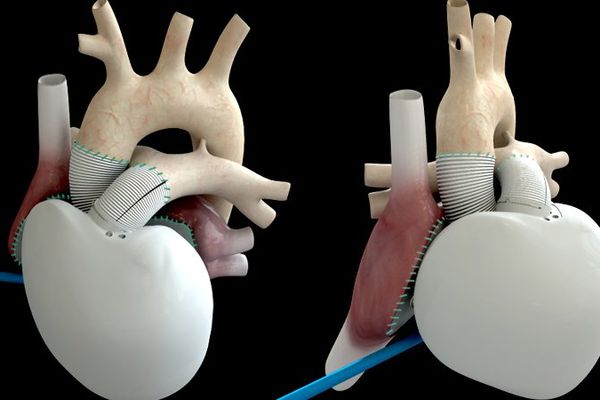
Le titre Carmat souffrait en Bourse, après que la société française a annoncé mardi 15 janvier avoir pris du retard dans l'essai clinique décisif sur son coeur artificiel total, le temps d'apporter de nouvelles améliorations sur la sécurité de sa prothèse. Le premier patient a été implanté à Nantes.
Carmat a annoncé dans un communiqué vouloir désormais soumettre "début 2020" son dossier de "marquage CE", alors qu'elle espérait jusqu'à présent décrocher ce feu vert commercial européen dès cette année. Son action perdait 7,49% à 24,7 euros mardi 15 janvier vers 13H00 à la Bourse de Paris, pendant que le CAC 40 était stable.
La baisse du titre est très probablement liée à ce report de calendrier, a estimé Romain Zana, analyste chez Exane BNP Paribas interrogé par l'AFP. Cependant, "dans un projet comme celui-ci, un report de calendrier de quelques mois est plutôt secondaire par rapport à un problème clinique", a-t-il relativisé.
Les problèmes techniques pointés par Carmat semblent mineurs, et d'ailleurs les premiers résultats cliniques de l'étude dite "pivot" en cours sont "plutôt encourageants", a ajouté Romain Zana.
"Actions correctives"
La production des prothèses et par conséquent les implantations dans le cadre de l'essai pivot ont été suspendues au quatrième trimestre 2018, car des "actions correctives" étaient nécessaires pour améliorer le processus de fabrication,"essentiellementsur le contrôle de l'intégrité et de la propreté du compartiment technique de laprothèse", selon Carmat.La production a repris récemment et les nouvelles prothèses seront disponibles dès avril. Les implantations pourront ainsi reprendre "début avril" au plus tard, a estimé Stéphane Piat, directeur général de Carmat, lors d'une conférence de presse mardi 15 janvier à Paris.
Lors de son précédent point d'étape, fin septembre, la société française avait réitéré son objectif d'implanter le dernier patient de son étude clinique pivot d'ici fin décembre 2018, afin de déposer et obtenir le marquage réglementaire européen courant 2019.
Les débuts de cette étude avaient déjà été mouvementés. Le premier patient, implanté à Nantes à l'été 2016, était décédé quelques mois après, en raison d'une mauvaise manipulation de sa part des batteries alimentant sa prothèse, selon Carmat.
La société avait par conséquent dû suspendre son essai pendant de longs mois, le temps de renforcer la sécurité de son dispositif et de convaincre l'Agence nationalede sécurité du médicament (ANSM).
Depuis fin 2017, Carmat a repris son essai à l'étranger, au Kazakhstan puis en République tchèque, et a aussi reçu des autorisations au Danemark. Carmat "est en train de valider des centres cliniques additionnels dans deux autres pays supplémentaires" afin de pouvoir finaliser "rapidement" le recrutement des derniers patients de cette étude, devant porter sur 20 patients au total, selon le communiqué.
Résultats intermédiaires "positifs"
Les résultats intermédiaires de cette étude sur dix premiers patients sont "positifs", a également souligné l'entreprise mardi. Car 70% de ces patients, tous atteints d'insuffisance cardiaque biventriculaire terminale, ont atteint l'objectif primaire de l'étude, selon la société. Cet objectif principal correspond à un taux de survie de six mois minimum avec la prothèse, ou à une transplantation cardiaque réussie dans les six mois suivant l'implantation du dispositif de Carmat.Trois patients sur les dix premiers de l'étude ont subi avec succès une greffe de coeur dans les délais impartis, a précisé mardi 15 janvier Stéphane Piat.
"Ces données intermédiaires confirment que notre coeur bioprothétique respecte la physiologie du corps humain et permet d'éviter les complications habituelles rencontrées avec d'autres technologies", selon le directeur général.
Carmat a aussi assuré mardi disposer des "ressources financières nécessaires pour soutenir ses développements cliniques et industriels et préparer la phase commerciale" en Europe à horizon 2020.
Revenue à 25,2 millions d'euros, sa trésorerie au 31 décembre 2018 a fondu de 43% par rapport au 30 juin mais l'entreprise peut encore activer, au cours des 36 prochains mois, jusqu'à 24,2 millions d'euros de lignes de "financement flexible", en fonds propres, mises en place avec Kepler Cheuvreux, et a par ailleurs récemment obtenu un accord de prêt de 30 millions d'euros de la part de la Banque européenne d'investissement(BEI).
La société a par ailleurs toujours bon espoir de pouvoir lancer un premier essai clinique aux Etats-Unis cette année, dans l'optique d'accéder à terme au marché commercial américain.