Ce lundi s’ouvre la semaine nationale de l’hémochromatose, l'occasion pour les associations de malades de sensibiliser à cette maladie due à un excès de fer dans l’organisme. Prise en charge tôt, elle se soigne facilement. D’où l’importance d’un dépistage précoce.
"A l’époque, tous les ans, entre février et mai, j’étais crevé mais je ne m’affolais pas. Et puis une année, je suis allé consulter et j’ai fait un bilan sanguin"… Philippe David avait 42 ans quand on a découvert un excès de fer dans son organisme, puis posé le diagnostic d’une hémochromatose. La quarantaine, l’âge classique auquel la maladie est détectée chez les hommes. Chez les femmes, c’est plutôt 50 ans car, avant, elles éliminent une partie de ce trop-plein de fer par les règles, les grossesses (gourmandes en fer) et l’allaitement.
Silence de la pathologie
Dès leur naissance les personnes atteintes d’hémochromatose absorbent environ quatre fois plus le fer que des personnes saines. Le fer est apporté dans l’organisme uniquement par l’alimentation. Chez une personne quelconque, seuls 10% du fer passent dans l’organisme, le reste est éliminé par les selles. Chez un hémochromatosique, c’est 40 % du fer qui passe dans l’organisme. Le foie agissant comme une éponge, absorbe, absorbe jusqu’à l’excès. Au bout d’une quarantaine d’années, la surcharge devient dangereuse. Le foie s’abîme et peut présenter une cirrhose voire un cancer.
Si certains malades ressentent des symptômes, comme de la fatigue, des douleurs articulaires ou des troubles cardiaques, d’autres ne perçoivent aucun signe. Et le danger réside dans ce silence de la pathologie. Pour certains patients, la prise en charge s’avère trop tardive.
Une mutation génétique celte
En Bretagne, six personnes sur 1000 sont porteuses de cette anomalie chromosomique pouvant conduire au développement de la maladie. "Dans 90% des cas, les femmes atteintes par cette mutation génétique, ne développeront jamais la maladie. Et 25% des hommes en déclareront une forme sévère", analyse le professeur Pierre Brissot, ancien responsable de recherche à l’INSERM (Institut National de la Santé et de la Recherche Médicale) dans l’unité "fer et foie ".
Ancien chef du service des maladies du foie au CHU de Rennes, Pierre Brissot a consacré sa vie au foie et à l’hémochromatose. Professeur émérite de médecine et membre titulaire de l’Académie nationale de médecine, il milite aujourd’hui au sein de la FFAMH (Fédération Française des Associations de Malades de l’Hémochromatose).
A l’origine de ce syndrome, une mutation génétique chez les peuples celtes. L’évolution géographique de la maladie suit d’ailleurs la migration des Celtes. "Mais sans chiffres sur le reste du territoire français, il s’avère impossible d’affirmer que cette maladie sévit plus en Bretagne qu’ailleurs, comme on l’entend souvent", constate Pierre Brissot. En revanche, on sait que c’est essentiellement chez le type caucasien qu’on retrouve cette mutation.
L’hémochromatose est une maladie récessive : pour en être atteint, il faut avoir deux chromosomes "mutants", l’un venant du père, l’autre de la mère. Les parents pouvant être porteurs sains et ne jamais développer la maladie. A l’inverse, comme on ne transmet que la moitié de son patrimoine génétique à ses enfants, il faut que l’autre membre du couple soit aussi porteur de cette anomalie chromosomique pour que les enfants aient des risques d’être malades.
Le traitement : la saignée
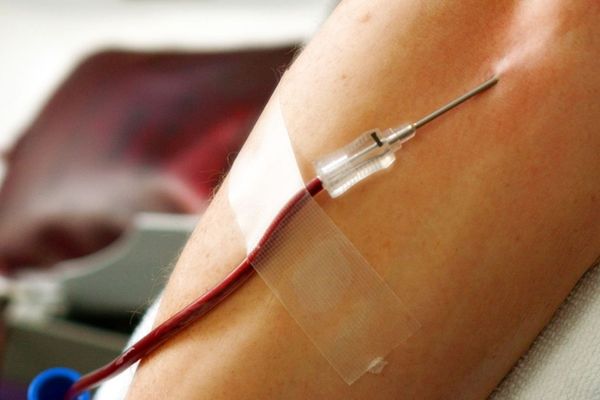
Le dépistage de la maladie se fait en premier lieu par une prise de sang qui révèle un taux anormalement élevé de fer. Puis d’autres examens viennent affirmer ou infirmer le diagnostic. Le premier traitement va être de désaturer l’organisme de cet excès de fer. Une série de saignées quasiment hebdomadaires se met alors en place pendant 6 mois à un an.
Une fois, un taux de fer normal retrouvé, les patients continuent les saignées. Selon les cas, leur nombre varie de trois à six par an avec des prélèvements d’environ 500 ml à chaque fois. Pour l’instant la saignée demeure le seul remède connu pour l’hémochromatose.
Les difficultés du parcours de soin
Jusqu’en 2019, les établissements français du sang (EFS) étaient habilités à effectuer les saignées." Aujourd’hui, suite à des arbitrages budgétaires, ils ne prennent plus que le sang qu’ils peuvent utiliser. Cela ne concerne donc que 30% des patients", détaille Joël Demares, président de l’association hémochromatose Ouest (AHO), présente en Bretagne et Pays de Loire.
Le reste des malades se partage entre hôpital et infirmiers libéraux. Mais beaucoup d’hôpitaux n’acceptent pas de pratiquer des saignées faute d’équipements adaptés ou tout simplement parce que le tarif d’une saignée s’avère trop faible.
Quant aux infirmiers libéraux, ils reçoivent 18.25 € à chaque saignée pour des actes qui durent entre un quart d’heure et une heure, selon le débit sanguin du patient. Si se débarrasser du sang en ville n’est pas un problème, puisque les collectes y sont organisées, cette opération est impossible en campagne. Aucun circuit de ramassage des poches de sang, considérées comme des déchets d’activités de soins à risques infectieux (DASRI), n’existe.
"Il faut développer les saignées à l’hôpital et en clinique", assène le professeur Pierre Brissot. "On se bat pour revaloriser l’acte des infirmiers libéraux", poursuit Joël Demares. Malgré nos sollicitations, l’ARS (Agence régionale de santé) n’a pas répondu à nos questions.
"Après chaque saignée, l’organisme va réagir en voulant se réapprovisionner rapidement en fer et va tenter d’en absorber plus", observe Pierre Brissot. Cette réaction physiologique, les chercheurs aimeraient l’éviter en n’ayant plus recours aux saignées. Des solutions médicamenteuses sont donc à l’étude.
Recherche
La collaboration entre le CHU de Rennes et le groupe "fer et foie" de l’INSERM de Rennes a abouti à des découvertes fondamentales sur l’hémochromatose.
En 1976, le caractère génétique de la maladie est mis en évidence au centre hospitalier de Pontchaillou à Rennes par le professeur Marcel Simon, sans pour autant trouver la mutation génétique en cause.
Ce n’est que 20 ans plus tard, en 1996, qu’une équipe américaine identifie le gène responsable de la maladie.
Puis, à nouveau à Rennes, en 2001, le chercheur, Olivier Loréal, de l’INSERM fait une découverte majeure : il met au jour le rôle d’une protéine du foie l’hepcidine dans le métabolisme du fer.
En quantité insuffisante chez le malade hémochromatosique, elle entraîne une hyperabsorption de fer. Alors pourquoi ne pas supplémenter les patients en hepcidine? Et bien parce 20 ans après cette découverte, la molécule, petite et complexe, reste difficilement synthétisable. Néanmoins, les études expérimentales chez l’animal sont prometteuses et les tout premiers essais cliniques ont débuté.
Autre piste intéressante : la ferroportine. Cette protéine aide le fer à traverser la paroi intestinale pour rejoindre le sang de l’organisme (et donc les organes). Diminuer la quantité de ferroportine se révèle une piste à explorer. "C’est balbutiant, expérimental, mais c’est une des voies d’avenir", conclut le professeur Brissot.