Le 31 mars, le CHU d'Amiens devait débuter l'essai clinique européen Discovery pour tester 4 traitements expérimentaux contre le Covid-19. Des tests reportés à cause du manque d'un médicament : le Remdesivir. Par contre, l'étude Hycovid visant à évaluer l'efficacité de la chloroquine a pu commencer.
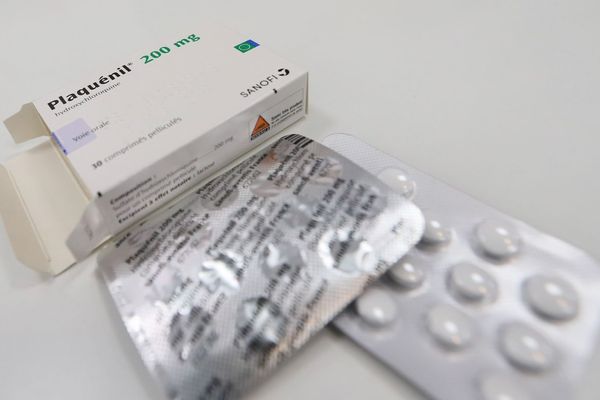
Jusqu’alors engagé uniquement dans des projets de recherches non thérapeutiques en lien avec le coronavirus, le CHU d’Amiens a intégré mercredi 1er avril l’étude Hycovid destinée à évaluer l’efficacité d’une molécule qui suscite autant d’espoir que de controverse : l’hydroxychloroquine plébiscitée par le professeur Didier Raoult, directeur de l’Institut hospitalo-universitaire de Marseille.
Face à l’urgence sanitaire, l’étude Hycovid, initiée par le CHU d’Angers, a pour objectif de répondre rapidement mais très scientifiquement à cette question : « Oui ou non, l’hydroxychloroquine est-elle efficace chez les patients atteints de Covid-19 à haut risque d’aggravation ? »
Pour y parvenir, le CHU d’Angers, en collaboration avec 36 hôpitaux français dont le CHU d’Amiens et les centres hospitaliers de Tourcoing et de Valenciennes, a décidé de lancer cette étude à grande échelle qui va concerner 1300 patients dans toute la France.
Seuls les patients atteints d’une "forme non sévère de Covid-19 mais à risque élevé d’évolution défavorable" seront inclus dans cette étude. Seront donc ciblés exclusivement les malades âgés de plus de 75 ans ou ayant besoin d’oxygène sans être en détresse respiratoire aiguë.
Hydroxychloroquine ou placébo
"A Amiens, 5 malades ont d’ores et déjà été inclus dans cette étude Hycovid. Mais au fil des jours, le nombre de patients concernés va naturellement augmenter", explique le professeur Jean-Luc Schmit, chef du service Pathologies infectieuses et tropicales et responsable des unités Covid-19 au CHU d’Amiens.
L'étude Hycovid est très simple mais indiscutable scientifiquement : "Parmi les patients tirés au sort et qui auront donné leur accord, la moitié se verra administrer l’hydroxychloroquine alors que l’autre moitié recevra un placebo, semblable en tous points à la molécule testée mais sans aucun principe actif. Et ni les patients, ni les médecins ne sauront si le patient reçoit de la chloroquine ou un placebo. C’est ce qu’on appelle ‘un essai à deux bras en double aveugle'", précise le Pr Schmit.L’efficacité du médicament sera jugée 14 jours après le début du traitement, en comparant le nombre de patients décédés ou transférés en service de réanimation en raison d’une aggravation respiratoire. Et les premiers résultats significatifs sont attendus entre 20 jours et quelques semaines.
Une étude Hycovid qui, dès son lancement le 1er avril, a suscité de nombreuses réactions dans la communauté médicale notamment car, contrairement au protocole prôné par le professeur Raoult, elle ne teste que l’hydroxycloroquine seule et pas son association avec l’antibiotique azythromycine.
L’étude #hycovid ne répondra pas aux questions car:
— Rachid Bahi (@docteurbahi) April 2, 2020
- patients >75ans
- dosage hydroxychloroquine 400mg (contre 600mg chez @raoult_didier)
- pas d’azithromycine#COVID19 #COVID19fr #COVID2019france
Un début de polémique auquel le CHU d’Angers a tenu à répondre rapidement par l’intermédiaire d’une foire aux questions consacrée à l’étude Hycovid, expliquant notamment que l’association entre l’hydroxycloroquine et l’azythromycine présentait « un risque élevé de toxicité cardiaque ».
A Amiens, Discovery reporté à cause d’un manque de médicaments
En parallèle à cette étude française Hycovid, le CHU d’Amiens devait également prendre part dès le 31 mars à l’essai clinique européen baptisé Discovery - et coordonné en France par l'Inserm, l'Institut national de la santé et de la recherche médicale - qui vise à tester 4 traitements distincts sur 3200 patients dans 7 pays, dont 800 en France. Un programme .Eh bien il faudra encore attendre un peu… Faute de médicaments disponibles. En effet, selon le professeur Schmit : "le CHU d'Amiens n'a pas encore été livré en Remdesivir", une molécule antivirale conçue initialement pour traiter le virus Ebola et qui est fabriquée exclusivement par le laboratoire américain Gilead basé en Californie.
"Nous attendons la livraison en provenance des Etats-Unis pour le début de la semaine prochaine, lundi 6 ou mardi 7 avril", espère le professeur Schmit. "Sans cette molécule, impossible de commencer ! Il faut que l’on puisse avoir accès aux 4 traitements avant de lancer les essais cliniques car là encore, tout est tiré au sort : le patient comme le traitement qu’il va tester."
De son côté, le laboratoire américain Gilead explique avoir déjà "mis à disposition de l'Inserm les 200 traitements Remdisivir" initialement prévus pour mener l'étude Discovery en France. "L'Inserm nous ayant demandé cette semaine de lui fournir 100 traitements supplémentaires, nous avons répondu positivement à cette demande et les médicaments seront livrés dans les plus brefs délais, comme convenu avec l'Inserm".
Contrairement à l’étude Hycovid, cet essai clinique Discovery coordonné par l’Inserm (Institut national de la santé et de la recherche médicale) est réservé aux patients touchés par des formes sévères du Covid-19. Il est en outre beaucoup plus complexe que l’étude Hycovid, car il ne comporte pas deux mais cinq "bras" de traitement :
- soins standards,
- soins standards + Remdesivir, conçu à l’origine pour traiter Ebola,
- soins standards + la combinaison Lopinavir et Ritonavir, initialement utilisée pour traiter le VIH,
- soins standards + la combinaison Lopinavir et Ritonavir associée à l’interféron beta pour stimuler les défenses immunitaires,
- soins standards + Hydroxychloriquine, normalement utilisé pour traiter la polyarthrite rhumatoïde ou le lupus.
Mais comme l’étude Hycovid, cet essai clinique Discovery rencontre de nombreux détracteurs parmi ceux qui défendent les thèses du professeur Raoult, notamment car il ne s’adresse qu’aux malades dans un état grave alors que l’infectiologue marseillais défend une administration de l’hydroxychloroquine dès le début des symptômes.
"C'est quand ils ont des formes modérées, moyennes, ou qui commencent à s'aggraver, qu'il faut les traiter. A ce moment là on contrôle les virus qui se multiplient. Quand ils sont rentrés en réanimation, le problème ce n'est plus le virus". (2/2)https://t.co/PT6xrsqH4z
— Didier Raoult (@raoult_didier) March 25, 2020
Alors pourquoi réserver cet essai aux malades les plus graves ? France 3 Bourgogne Franche-Comté a obtenu la réponse à cette question auprès du professeur Lionel Piroth, infectiologue qui coordonne le projet Discovery au CHU de Dijon : "Ces traitements ont tous des effets indésirables. L’acceptation des effets indésirables sera d’autant plus large que l’état du patient est grave. La majeure partie des patients qui vont faire une infection à Covid vont guérir spontanément. Pourquoi leur faire subir un traitement à effets indésirables alors qu’ils vont guérir ?"
L’analyse de l’efficacité des traitements testés par Discovery sera effectuée 15 jours après l'inclusion de chaque patient mais vu le nombre de patients et de pays concernés, les résultats définitifs de ces essais cliniques ne seront pas connus avant plusieurs mois. Des premiers enseignements pourraient cependant être tirés dans les semaines à venir.

/regions/2020/06/09/5edf987c31c72_maxnewsfrfour409980-4742502.jpg)