Ce décontractant musculaire à base de tétrazépam causerait des réactions cutanées rares mais très graves et parfois mortelles.
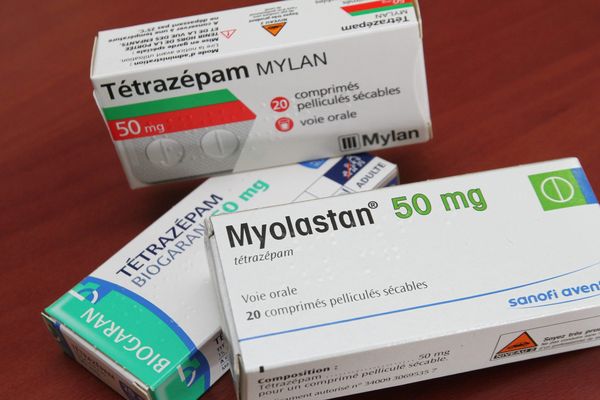
Après des anti-inflammatoires, cette fois, c'est un décontractant musculaire à base de tétrazépam qui sera retiré. Le Myolastan et ses génériques, un médicament utilisé dans le traitement des contractures musculaires douloureuses en rhumatologie, sera interdit à partir du lundi 8 juillet en France. Les malades chroniques du dos qui avaient l'habitude de le prendre pour tenter d'apaiser leurs douleurs sont inquiets. Cette suspension sera accompagnée le même jour d'un rappel de toutes les boîtes disponibles sur le marché, précise l'agence du médicament, l'ANSM.
Des réactions cutanées rares mais très graves et parfois mortelles sont à l'origine de cette suspension du marché. Cette suspension du marché des médicaments à base de tétrazépam (Myolastan du laboratoire Sanofi et ses génériques: Panos de Daiichi Sankyo France, Tetrazepam d'Arrow, Sandoz, Biogaran, etc.), se fait "en accord avec les autorités européennes".
Voir le reportage
Suspension effective à partir du 8 juillet 2013
Cette suspension sera effective à partir du 8 juillet 2013 et un rappel des lots disponibles sur le marché français
sera effectué à cette date.
En accord avec l’ANSM, les laboratoires concernés adressent un courrier aux professionnels de santé concernés
comportant des informations importantes quant à cette suspension.
Recommandations de l’ANSM
Il est recommandé aux prescripteurs de :- ne plus instaurer ni renouveler de traitement par tétrazépam. Au vu de l’indication et des données d’utilisation en France, le tétrazépam est utilisé sur de courtes périodes ; aussi, la problématique du sevrage ne devrait pas se poser pour cette benzodiazépine. Dans les cas exceptionnels d’utilisation au long cours, un risque de syndrome de sevrage ne peut cependant pas être exclu ;
- informer les patients traités de la suspension de l’AMM des médicaments contenant du tétrazépam ;
- réexaminer le traitement de leurs patients lors de la prochaine visite afin d’arrêter le traitement par tétrazépam et d’envisager une alternative thérapeutique appropriée.
- informer les patients traités de la suspension des AMM des médicaments contenant du tétrazépam et de l’indisponibilité de ces spécialités à partir du 08 juillet 2013 ;
- orienter les patients en cours de traitement avec tétrazépam vers leur médecin afin de l’arrêter et d’envisager une alternative thérapeutique appropriée.